Mở đầu
35
Tại sao giấm ăn, nước chanh… đều có vị chua và được dùng để loại bỏ cặn trong dụng cụ đun nước?
Đáp án
Giấm ăn, nước quả chanh, … đều có vị chua và được dùng để loại bỏ cặn trong dụng cụ đun nước do đều có chứa acid.
35
Tại sao giấm ăn, nước chanh… đều có vị chua và được dùng để loại bỏ cặn trong dụng cụ đun nước?
Giấm ăn, nước quả chanh, … đều có vị chua và được dùng để loại bỏ cặn trong dụng cụ đun nước do đều có chứa acid.
35
Tìm hiểu khái niệm acid
Bảng 8.1. Tên một số acid thông dụng, công thức hoá học và dạng tồn tại của acid trong dung dịch
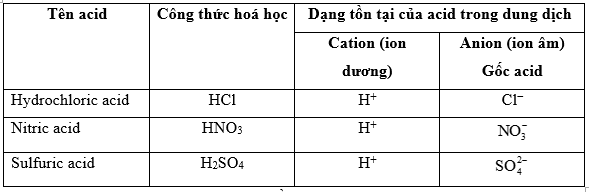
Quan sát Bảng 8.1 và thực hiện các yêu cầu sau:
1. Công thức hoá học của các acid có đặc điểm gì giống nhau?
2. Dạng tồn tại của acid trong dung dịch có đặc điểm gì chung?
3. Đề xuất khái niệm về acid.
1. Công thức hoá học của các acid đều có chứa nguyên tử H.
2. Dạng tồn tại của acid trong dung dịch đều chứa cation (ion dương) \(H^+\).
3. Acid là những hợp chất trong phân tử có nguyên tử hydrogen liên kết với gốc acid. Khi tan trong nước, acid tạo ra ion \(H^+\).
36
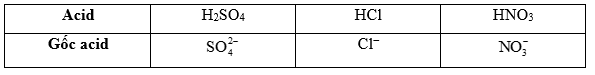
Hãy cho biết gốc acid trong các acid sau: \(H_2SO_4, HCl, HNO_3\)
36
Tính chất của dung dịch hydrochloric acid
Chuẩn bị: dung dịch HCl 1 M, giấy quỳ tím; hai ống nghiệm mỗi ống dựng một trong các kim loại Fe, Zn, ống hút nhỏ giọt.
Tiến hành:
- Nhỏ 1 – 2 giọt dung dịch HCl vào mẩu giấy quỳ tím.
- Cho khoảng 3 mL dung dịch HCl vào mỗi ống nghiệm đã chuẩn bị ở trên.
Mô tả hiện tượng xảy ra và viết phương trình hoá học.
- Nhỏ 1 - 2 giọt dung dịch \(\mathrm{HCl}\) vào mẩu giấy quỳ tím thấy mẩu giấy quỳ tím chuyển sang màu đỏ.
- Cho khoảng \(3 \mathrm{~mL}\) dung dịch \(\mathrm{HCl}\) vào từng ống nghiệm chứa \(\mathrm{Fe}\); Zn thấy kim loại tan dần, giải phóng khí không màu.
Phương trình hoá học:
\(\mathrm{Fe}+2 \mathrm{HCl} \rightarrow \mathrm{FeCl}_2+\mathrm{H}_2\)
\(\mathrm{Zn}+2 \mathrm{HCl} \rightarrow \mathrm{ZnCl}_2+\mathrm{H}_2\)
36
Cho dung dịch HCl tác dụng với kim loại Mg. Viết phương trình hoá học của phản ứng xảy ra.
Phương trình hoá học của phản ứng xảy ra:
\(Mg + 2HCl → MgCl_2 + H_2\)
37
Sử dụng Hình 8.1 để trình bày về các ứng dụng của sulfuric acid.
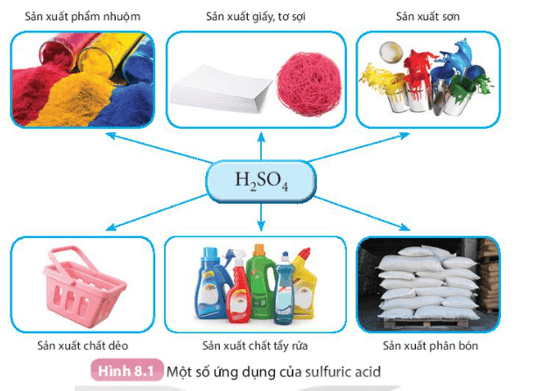
Một số ứng dụng của sulfuric acid:
- Sản xuất phẩm nhuộm;
- Sản xuất giấy, tơ sợi;
- Sản xuất sơn;
- Sản xuất chất dẻo;
- Sản xuất chất tẩy rửa;
- Sản xuất phân bón …
37
Sử dụng Hình 8.2 để trình bày về một số ứng dụng của hydrochloric acid.
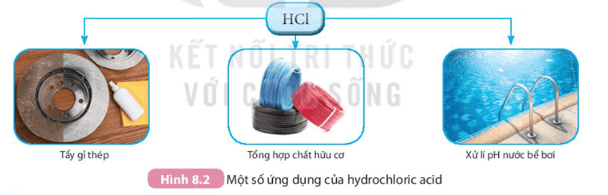
Một số ứng dụng của hydrochloric acid:
- Tẩy gỉ thép;
- Tổng hợp chất hữu cơ;
- Xử lí pH nước bể bơi …
38
Sử dụng Hình 8.3 để trình bày về các ứng dụng của acetic acid.
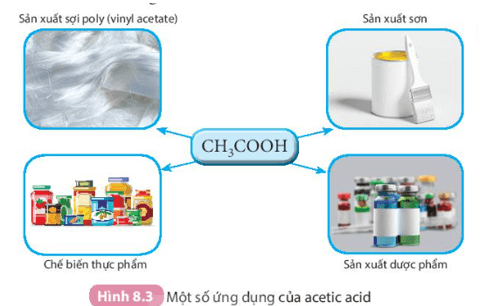
Một số ứng dụng của acetic acid:
- Sản xuất sợi poly (vinyl acetate);
- Sản xuất sơn;
- Chế biến thực phẩm;
- Sản xuất dược phẩm …
38
Hãy tìm hiểu về nhu cầu sử dụng và ứng dụng của một trong các acid sau: \(HCl, H_2SO_4, CH_3COOH\) và trình bày trước lớp.
- Nhu cầu sử dụng và ứng dụng của acid HCl:
Hiện nay, mỗi năm thế giới sản xuất hàng chục triệu tấn hydrochloric acid.
Lượng lớn hydrochloric acid được sử dụng để sản xuất vinyl chloride cung cấp cho ngành nhựa, ammonium chloride để cung cấp cho ngành sản xuất phân bón, các chloride kim loại để cung cấp cho ngành hoá chất, các hợp chất hữu cơ chứa chlorine để phục vụ sản xuất dược phẩm, thuốc nhuộm.
Ngoài ra, hydrochloric acid còn được dùng để trung hoà môi trường base hoặc thuỷ phân các chất trong quá trình sản xuất, tẩy rửa gỉ sét (thành phần chính là các iron oxide) bám trên bề mặt của các loại thép…
- Nhu cầu sử dụng và ứng dụng của acid \(H_2SO_4\):
Mỗi năm, cả thế giới cần đến hàng trăm triệu tấn sulfuric acid. Trong đó, gần 50% lượng acid được dùng để sản xuất phân bón như ammonium sulfate, calcium dihydrogenphosphate\((Ca(H_2PO_4)_2)\) … Acid này còn được sử dụng trong sản xuất chất tẩy rửa, sơn, phẩm màu, thuốc trừ sâu, giấy, chế hoá dầu mỏ, …
- Nhu cầu sử dụng và ứng dụng của acid \(CH_3COOH\):
Một lượng lớn acetic acid được sử dụng để sản xuất vinyl acetate và cellulose acetate. Vinyl acetate được dùng để sản xuất keo dán và chất kết dính trong sản xuất giấy, sản xuất tơ (tơ vinylon), …; cellulose acetate được sử dụng làm tá dược trong sản xuất thuốc, sản xuất tơ, phim ảnh …
Acetic acid còn được dùng để tổng hợp aluminium monoacetate \((Al(OH)_2COOCH_3)\) làm chất cầm màu trong công nghệ dệt may, tổng hợp ethyl acetate, butyl acetate làm dung môi (để pha sơn), tổng hợp muối ammonium acetate \((CH_3COONH_4)\) để sản xuất acetamide một chất có tác dụng lợi liểu và làm toát mồ hôi; tổng hợp phenylacetic acid dùng trong công nghiệp nước hoa, tổng hợp penicillin, tổng hợp chloroacetic acid dùng trong sản xuất chất diệt cỏ 2,4 – D và 2,4,5 – T, … Dung dịch acetic acid 2 – 5% được dùng làm giấm ăn, làm chất tẩy cặn trong siêu đun nước và nhiều ứng dụng trong cuộc sống hàng ngày.
38
Việc sử dụng acid không đúng cách sẽ gây ô nhiễm môi trường đất, nước, không khí. Em hãy tìm hiểu về các tác hại này và trình bày trước lớp.
Việc sử dụng acid không đúng cách sẽ gây ô nhiễm môi trường đất, nước, không khí. Cụ thể:
- Acid dư thừa sau sử dụng thải trực tiếp ra môi trường ngấm vào đất làm chua đất, làm rửa trôi các chất dinh dưỡng có trong đất … không những thế chúng còn làm cho cây trồng bị suy yếu và chết hàng loạt. Nhất là đối với những cây nông nghiệp (rau, củ, quả …) môi trường acid sẽ gây ra những thiệt hại lớn …
- Acid dư thừa sau sử dụng thải trực tiếp ra môi trường nước làm giảm độ pH của nước, khiến cho các loài sinh vật bị cản trở quá trình hấp thụ chất dinh dưỡng … Ngoài ra, các loài sinh vật sẽ bị hạn chế phát triển, chết dần và khó có thể tái tạo về môi trường sinh thái ban đầu. Đối với những người dân chuyên sống bằng nghề nuôi trồng và đánh bắt thủy hải sản, thì đây sẽ là một mối nguy cơ lớn gây ảnh hưởng tới đời sống kinh tế và sản xuất của người dân.
- Trong không khí các hạt acid lơ lửng gây ô nhiễm không khí, ảnh hưởng tới tầm nhìn xa trong không khí gây cản trở tới hoạt động nghiên cứu của các chuyên gia về khí tượng, môi trường…
- Đối với con người, khi da tiếp xúc với môi trường không khí bị ô nhiễm do acid sẽ gây ra các bệnh về da như mẩn ngứa, nấm, viêm da, gây mụn nhọt, mụn trứng cá… Sử dụng nước dư acid trong ăn uống còn gây ảnh hưởng tới hệ tiêu hóa, gây ra các bệnh về đường ruột như trào ngược dạ dày, đau dạ dày, ợ hơi, khó tiêu… Trẻ em sử dụng nước dư acid thường xuyên sẽ gây tổn hại cho hệ thần kinh, não bộ, thậm chí là tử vong. Về lâu dài, nước dư acid còn là nguyên nhân gây ra bệnh Alzheimer ở người già. Khi hít thở không khí có chứa các hạt bụi acid sẽ làm ảnh hưởng tới đường hô hấp và giảm sức đề kháng của cơ thể….